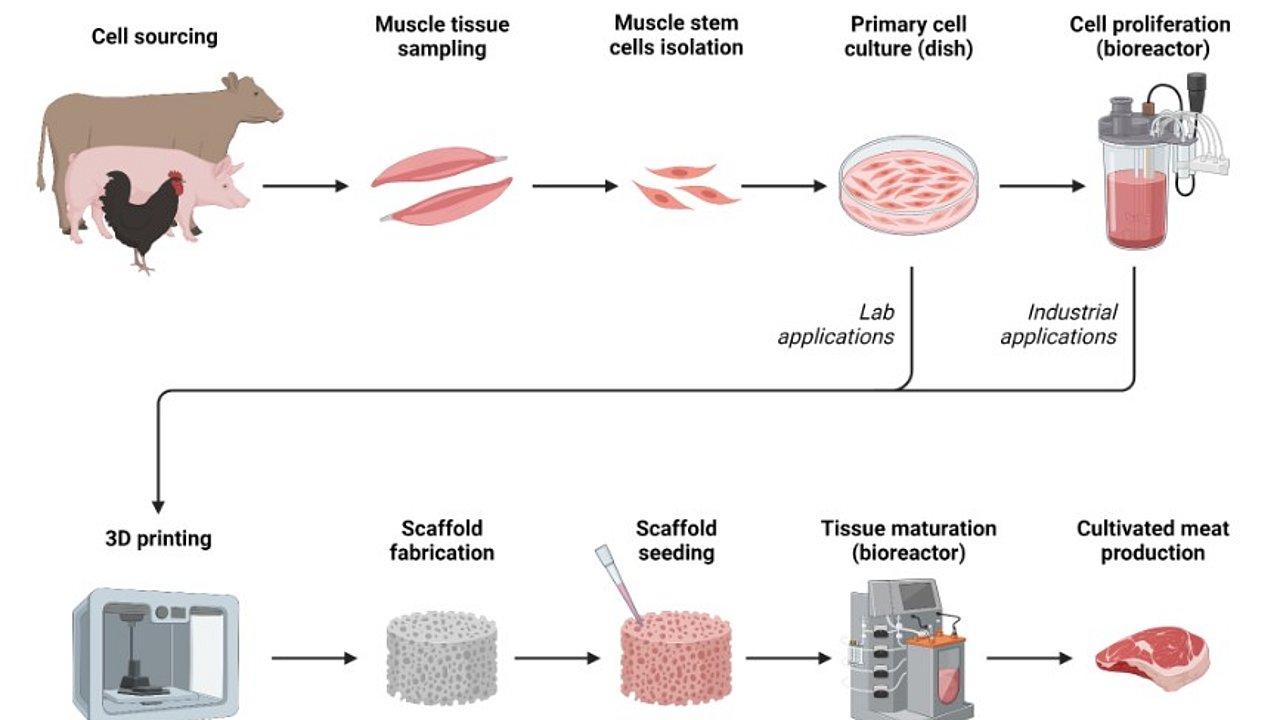
La carne coltivata è un prodotto alimentare innovativo ottenuto in laboratorio tramite l’isolamento di cellule staminali di animali, ad esempio bovini, polli, suini o pesci, che vengono fatte proliferare in vitro in condizioni controllate. Attraverso questo, processo, le cellule si moltiplicano e si differenziano, dando origine a una biomassa cellulare. Le cellule utilizzate per produrre la carne coltivata possono essere prelevate da animali vivi, tramite una piccola biopsia, oppure da tessuti provenienti da una mezzena dopo la macellazione. Dal punto di vista biologico, il principio alla base della carne coltivata è quello di sfruttare i normali meccanismi di crescita e rigenerazione del muscolo animale, trasferendoli da un contesto fisiologico in vivo a un ambiente controllato di laboratorio.
Contesto globale e motivazioni dello sviluppo
L’idea di produrre carne coltivata nasce come risposta a una combinazione di sfide globali: la crescita della popolazione mondiale che, secondo le stime delle Nazioni Unite, potrebbe raggiungere circa 10 miliardi di persone entro il 2050. L’aumento della popolazione comporterebbe una maggiore domanda di proteine di origine animale, richiedendo più terre e più animali, con conseguenti impatti ambientali e perdita di biodiversità. A queste si aggiungono motivazioni etiche legate, ad esempio, al benessere animale; oppure all’uso di antibiotici negli allevamenti. Durante la produzione di carne coltivata vengono inizialmente utilizzati antibiotici per prevenire eventuali contaminazioni microbiche; tuttavia, con il progresso delle tecniche produttive, il loro impiego tende a essere progressivamente ridotto, fino a essere eliminato. In questo contesto, la carne coltivata è proposta come possibile affiancamento alla carne tradizionale, in grado di offrire un prodotto che possa rispondere alla crescente domanda di proteine animali della popolazione. Inoltre, essa offre il potenziale vantaggio di garantire un prodotto maggiormente controllabile dal punto di vista igienico e nutrizionale.
Evoluzione storica del concetto di carne coltivata
Dal punto di vista storico, il concetto di carne prodotta in laboratorio fu anticipato già nel 1931 dal politico britannico Winston Churchill, che nel saggio “Cinquant’anni da oggi” immaginava un futuro in cui si sarebbe potuta evitare – scriveva – «L’assurdità di allevare un pollo intero per poi mangiarne solo il petto o l’ala, facendo crescere queste parti separatamente in un mezzo adatto». Una tappa fondamentale si è avuta nel 2013, quando il professor Mark Post dell’Università di Maastricht presentò a Londra il primo hamburger di carne coltivata, ottenuto a partire da cellule muscolari bovine e costato oltre 250.000 euro, dimostrando però la fattibilità del concetto su scala sperimentale.
Cellule immortalizzate e implicazioni per la scalabilità
I primi esperimenti che si stanno svolgendo per la carne coltivata vengono utilizzati linee cellulari immortalizzate (ovvero modificate geneticamente per superare i limiti naturali di replicazione, dividendosi indefinitamente). Tra le linee cellulari più utilizzate nella ricerca biotecnologica figurano la linea mioblastica murina C2C12, derivata dal muscolo scheletrico di topo, e la linea epiteliale CHO (Chinese Hamster Ovary) derivata dalle ovaie del criceto cinese. Queste linee cellulari sono ampiamente impiegate come modelli sperimentali per studiare i meccanismi di proliferazione, differenziazione e metabolismo cellulare, e rappresentano strumenti fondamentali nello sviluppo delle tecnologie di agricoltura cellulare. L’utilizzo di cellule immortalizzate è considerato particolarmente vantaggioso al fine della scalabilità industriale della carne coltivata. A differenza delle cellule primarie, che presentano un numero limitato di cicli replicativi prima di entrare in senescenza, le cellule immortalizzate possono essere coltivate per lunghi periodi e permettono di ottenere una fonte cellulare stabile e riproducibile per la produzione su larga scala. Nonostante questi vantaggi, l’impiego di linee cellulari immortalizzate solleva diverse questioni scientifiche, di sicurezza, regolatorie ed etiche. In primo luogo, molte strategie di immortalizzazione prevedono modificazioni genetiche o l’attivazione di geni coinvolti nel controllo del ciclo cellulare, come l’espressione della telomerasi o di oncogeni virali. Questo aspetto richiede valutazioni approfondite per garantire che i prodotti derivati da tali cellule non presentino effetti indesiderati per il consumatore. Un’altra sfida riguarda la limitata disponibilità di linee cellulari immortalizzate provenienti da specie animali comunemente consumate. Attualmente molte linee cellulari disponibili derivano da specie modello utilizzate nella ricerca, mentre esistono ancora poche linee cellulari sviluppate specificamente per applicazioni alimentari. Lo sviluppo e la caratterizzazione di nuove linee cellulari sicure, stabili e idonee alla produzione industriale rappresentano quindi una delle principali priorità per il progresso della carne coltivata. Infine, l’utilizzo di cellule immortalizzate pone sfide regolatorie, poiché molti sistemi normativi non dispongono ancora di un quadro legislativo specifico per gli alimenti ottenuti tramite agricoltura cellulare. Le autorità regolatorie devono quindi definire criteri per la valutazione della sicurezza, della stabilità genetica e della tracciabilità delle linee cellulari utilizzate nella produzione di carne coltivata. Alimentare e sostenere la proliferazione delle cellule per la carne coltivata richiede l’uso di mezzi di coltura specifici. Una volta isolate le cellule dal tessuto muscolare o tramite biopsia, queste vengono coltivate in ambienti che forniscono tutti i nutrienti necessari, tra cui amminoacidi essenziali, vitamine, sali minerali, glucosio, oltre a fattori di crescita, antibiotici e siero fetale bovino (FBS) derivato dal sangue dei feti bovini. Per motivi etici e di sostenibilità, si stanno sviluppando alternative al FBS, come sieri sintetici o estratti vegetali, che permettono di evitare l’uso di derivati animali pur mantenendo la proliferazione cellulare.
Principali fattori di crescita utilizzati
Per far aumentare le cellule in laboratorio e ottenere una biomassa, le cellule hanno bisogno di “segnali” che dicano loro come crescere, moltiplicarsi e differenziarsi. Questi segnali sono forniti dai fattori di crescita
I principali fattori di crescita utilizzati nella carne coltivata sono:
Fattori di crescita dei Fibroblasti (FGF) - stimolano le cellule muscolari a proliferare, cioè a moltiplicarsi, mantenendole attive durante le prime fasi della coltura;
Fattori di Crescita Insulino-simili (IGF-1 e IGF-2) - guidano le cellule verso la differenziazione, aiutandole a trasformarsi in fibre muscolari organizzate, proprio come succede nel muscolo vivo;
Fattore di Crescita Derivato dalle Piastrine (PDGF) – supporta la proliferazione cellulare e il reclutamento di cellule di supporto;
Fattore di Crescita degli Epatociti (HGF) – Attiva le cellule satellite muscolari e ne stimola la migrazione e proliferazione nelle fasi iniziali della rigenerazione.
L’uso combinato di questi fattori permette di ricreare in laboratorio l’ambiente biologico naturale del muscolo, guidando le cellule dalla fase iniziale di isolamento fino alla formazione di una biomassa cellulare. In pratica, i fattori di crescita sono come istruzioni biologiche che indicano alle cellule quando crescere, come disporsi e quando differenziarsi, rendendo possibile alla produzione di una biomassa cellulare che è il primo step per la produzione della carne coltivata.
Dalla coltura in vitro ai bioreattori industriali
Le cellule vengono coltivate inizialmente in incubatori da laboratorio, a temperature di 37°C e 5% di CO₂. Per passare da una produzione sperimentale a una scala industriale è necessario trasferire la biomassa cellulare in bioreattori, che consentono di controllare in modo preciso parametri come pH, ossigenazione, temperatura e apporto di nutrienti. I bioreattori permettono inoltre di ottenere elevate densità cellulari e di standardizzare il processo produttivo, riducendo la variabilità tra lotti.
Struttura tridimensionale e ruolo degli scaffold
Per ottenere un tessuto che riproduca la struttura della carne tradizionale, la biomassa cellulare deve svilupparsi in tre dimensioni. A questo scopo vengono utilizzati gli scaffold, ovvero strutture tridimensionali costituite da biomateriali biocompatibili che fungono da impalcatura di supporto per l’adesione, l’allineamento e la proliferazione cellulare. Gli scaffold forniscono alle cellule un ambiente strutturale simile alla matrice extracellulare presente nei tessuti animali, favorendo la formazione di fibre muscolari organizzate e contribuendo allo sviluppo della texture del prodotto finale. Un approccio particolarmente promettente è rappresentato dall’utilizzo di scaffold decellularizzati, ovvero matrici biologiche da cui sono state rimosse le cellule originarie, lasciando intatta la struttura tridimensionale del materiale. Questo processo preserva l’architettura fibrosa e i componenti della matrice extracellulare, creando un ambiente favorevole all’adesione e alla crescita delle cellule muscolari coltivate. Gli scaffold decellularizzati possono essere ottenuti sia da tessuti animali, come muscolo o collagene, sia da strutture vegetali, come foglie o altri tessuti di piante. In questi ultimi, la rimozione delle cellule consente di mantenere una rete vascolare naturale, utile per la distribuzione dei nutrienti nelle colture cellulari. Uno degli esempi più studiati è rappresentato dalle foglie di spinacio decellularizzate, che conservano il loro scheletro vascolare e sono utilizzate come impalcatura per cellule. Queste cellule, grazie alla loro capacità proliferativa stabile nel tempo, hanno permesso di valutare la compatibilità e la funzionalità dello scaffold, mostrando elevata adesione e formazione di strutture simili a fibre muscolari dopo diverse settimane.
Arricchimento nutrizionale e proprietà sensoriali
Un aspetto cruciale della carne coltivata è l’arricchimento nutrizionale e sensoriale. La carne tradizionale contiene ferro eme, vitamine del gruppo B (in particolare B12), lipidi e pigmenti come la mioglobina, responsabili del colore rosso; nella carne coltivata questi elementi devono essere aggiunti. L’integrazione di cellule adipose o di grassi strutturati consente di migliorare succosità, aroma e percezione sensoriale, mentre la modulazione del profilo lipidico permette di ottenere prodotti con un contenuto di grassi più salutare rispetto alla carne convenzionale.
Bio-printing 3D e innovazioni tecnologiche
Un’ulteriore evoluzione tecnologica è rappresentata dal bio-printing 3D, che consente di depositare cellule e scaffold con estrema precisione spaziale, creando strutture complesse che imitano l’architettura del muscolo, inclusa la distribuzione del grasso (marbling). Variando le percentuali di cellule e materiali di supporto, è possibile modulare le proprietà meccaniche e sensoriali del prodotto finale, avvicinandolo sempre di più alla carne tradizionale.
Prospettive e sfide future
In conclusione, la carne coltivata rappresenta un’innovazione promettente e tra le più avanzate nel campo della produzione alimentare. Permangono tuttavia diverse sfide che i ricercatori stanno cercando di affrontare, legate a costi di produzione, scalabilità, regolamentazione e accettazione da parte dei consumatori. Parallelamente, è in corso un’analisi sempre più approfondita del prodotto finale, per valutarne qualità, sicurezza e caratteristiche nutrizionali.
IRCAF ringrazia Maria Antonietta Palumbo – dottoranda presso AGRISYSTEM dell’Università Cattolica del Sacro Cuore per il contributo a questo articolo